祝・日本神経科学学会50周年!
第48回日本神経科学学会大会
2025年7月24~27日に、新潟の朱鷺メッセで、第48回日本神経科学学会大会が行われました。
日本神経科学学会は、6,416名(2025年4月現在)の会員を擁する、日本最大の脳科学研究者の集まりで、世界的に見ても、30,000人以上の会員を擁する北米の神経科学会(Society for Neuroscience, SfN)に次ぐ、大規模な学会です。
僕が初めてこの学会に関わったのは、2007年、理研脳センター所属時に、同センターのグループディレクターであった田中啓治先生が第30回大会の大会長を務められた際に、運営に携わった時でした。実は当時僕は、日本神経化学会のメンバーではありましたが、神経科学学会の会員ではないのにうっかり実行委員に指名されてしまい、田中先生に、「え、会員じゃない!?」と言われてしまい、急いで入会しました次第です。その後、2011年にこの学会の理事になり、2013年には大会長を務め、2017~2019年にいったん理事を退任した後、柚崎通介会長、山中宏二理事長の2期の間、副会長、副理事長を務めるなど、深く関わってきた学会です。
2025年6月の理事会で、長く勤めた理事を退任して、やりきったような気になり、そろそろこの学会ともお別れだろうか…というような気持ちになりかけている中での参加でした。
大会スタート!
初日朝の最初の教育講演は、あの池谷裕二先生でした! 池谷先生のトークは、いつも通り、キレッキレでした。
今回、特に興味深かったのは、ラットの心拍バイオフィードバックの研究。まずは池谷先生ご自身が、心拍の数値を見ながら心拍を減らす訓練をする実験をされ、人間は確かに心拍を減らせることを示されました。そして、ラットに、心拍が減ると報酬が与えられるようにする訳です。そうすると、確かに、心拍減少を誘導できる。しかも心拍数を半分くらいに減らせてしまうのです。最初は血中の酸素飽和度が低下しますが、その後、次第に元に戻ります。なぜかというと、赤血球の数が代償的に増えたからなのですね。心拍が低下した後には、不安様行動が減少するなど、行動レベルにも変化が見られました。
さて、この心拍バイオフィードバックに必要な脳領域を探索した結果見つかったのが、前部帯状回(ACC)。心拍バイオフィードバックにより7Hzのθ帯域のオシレーションがACCで増加することがわかり、ACCを7Hz刺激すると心拍が減ることも判明。ACCと、その投射先である視床背内側核【配信時、視床腹内側核と記載しましたが、誤りでした。お詫びして訂正致します】のループが7Hzで共鳴するようです。最後に、視覚野からACCへの投射があることに着目し、7Hzの視覚刺激をすると、何と人の実験でも心拍が下がったとのこと。最後に会場に7Hzの刺激が流されましたが、この際、会場の皆の脈拍を測ったら一気に大規模な実験データがとれたかも?
終了後、心拍が下がるなら、血圧は下がりますか? もし血圧が下がるなら、医療応用はできますか?との質問もありました。確かに、高血圧が7Hzの光刺激で、薬なしで改善するなら、ありがたい話です。
好奇心に基づく研究と疾患研究の関係
ラットの心拍バイオフィードバックの研究は、おそらく、面白いからやってみよう、という感じで始められたものだと推測しますが、そういう研究が結果的に、役に立つこともある訳です。新たな医療を待つ患者さんが、研究者の飽くなき探究心、好奇心に基づく研究を見ると、今すぐ役に立つ研究をして欲しい、と思うかもしれません。しかし、高血圧を解明しよう、と研究していても、こんな結果にはたどり着かないでしょう。病気を解明したいと取り組んでいる研究者が何十年かけてもたどり着かなかった答えが、全く別の、好奇心に基づく研究からでることは、科学の歴史を見ると、枚挙に暇がありません。
例えば、今、遺伝子治療への応用が始まっているのが、2020年にノーベル賞を受賞した、画期的なゲノム編集技術、CRISPR/Cas9です。このCRISPRが発見されたきっかけは、元大阪大学微生物病研究所教授の中田篤男先生と、その研究室の石野良純先生のご研究です。中田先生は、大腸菌のアルカリフォスファターゼのアイソザイム(iap)には3種類の分子量の違うタイプがあり、これが1種類しかない変異体の研究をしてみよう、と思われたそうです。どうでしょう? これが病気の治療につながるとは、誰も思わないでしょう。石野先生は、この変異体のiap遺伝子に謎の繰り返し配列を発見しました。この繰り返し配列は、大腸菌ゲノムの中に他にも存在し、他の細菌からも見つかりました。 その後、繰り返し配列の間に、細菌を攻撃する病原体(バクテリオファージ)などの遺伝子断片が含まれている例が見つかり、この配列(CRISPR)が、外来のDNAから細胞を守る働きをしていることがわかったのです。この、繰り返し配列のスキマにあったDNAと同じ配列のDNAを切断することで、病原体を排除していたのです。
このように、研究者が自由な研究を行うことが学問の幅を広げ、病気の原因解明、新規治療法につながる面があるので、自由な学問の場は本当に貴重なのです。
50周年記念イベント
1974年に設立されたこの学会の50周年を祝して、今大会では、50周年記念イベントが大々的に行われました。
会場では、アートデザイン展「脳科学とアート」も開かれ、脳や神経細胞に触発されてアーティストが生み出した数々の作品が展示され、壮観でした。河口洋一郎氏の「Growth」(リンク先に写真があります)など、素晴らしい作品群でした。(脳科学とアートに関するクラウドファンディングも行われています。)
この展示には、「幻のカバーアート」コーナーもありました。下記は、この展示に最も多くの作品を提供された、東北大学の松井広先生のTweetです。

第48回日本神経科学大会第4会場 (203&204)
アートデザイン展「脳科学とアート」「幻のカバーアート展」研究内容にインスピレーションを得て、アートに昇華したものを展示。全26点の展示作品のうち、当研究室の作品が9点を占めました。
jnss.org/50th_memorial_…
幻のカバーアートというのは何かと言うと、メジャーな雑誌に論文が受理されると、「カバーに適したイラストや写真があれば送って下さい」というようなことが書かれているのです。もちろん、自分で作る人もいますが、プロのイラストレーターの方に依頼する人もいます。しかし! それが採用されるとは限らないのです…。そこで、採用されなかったイラストの展覧会が行われたという訳です。さすがにどれも気合いが入っていました。
さて、3日目には、創立50周年記念シンポジウムが行われ、僭越ながら僕が、この50年の日本神経科学学会における疾患領域の研究を展望しましたので、その内容をご紹介します。
日本神経科学学会における疾患研究の歩み
そもそも、神経科学の始まりは、病気の研究です。1861年、ブローカが発表した失語症を呈した症例の剖検脳の研究が、大脳皮質の機能局在研究の始まりだったのです。
さて、この学会の1978年の第1回学術集会は日本語のみ。病気の研究のセクションはありませんでした。

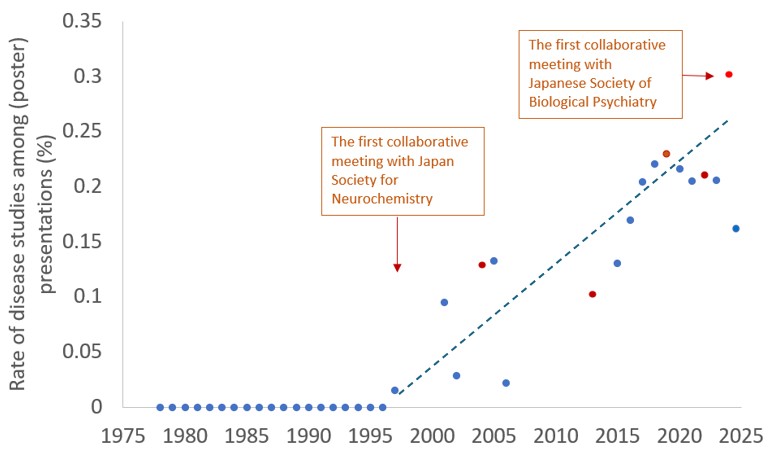
初めて病気のセクションができたのは、1997年の大会で、タイトルは「臨床神経学」。たった6題のセクションでした。しかし、その後、日本神経学会における疾患関連の演題数は、うなぎ登りに増えていきます。そのきっかけとなったのが、1998年に、初めて日本神経化学会との合同大会が開かれたことです。
日本神経化学会のルーツは、1958年に、日本精神神経学会で発足した「神経化学、体液病理懇話会」。その後、幅広い分野の基礎研究者が参加し、1966年に日本神経化学会(Japanese Society for Neurochemistry)となりましたが、今も、精神・神経疾患の分子基盤に関心を持つ研究者が集まっています。日本神経科学学会が、およそ4年に1回程度の頻度で、日本神経化学会との合同大会を、(多くは神経回路学会とも合同で)「Neuro」と称して開催してきたことが、疾患研究の増加につながってきたと思われます。
そんな神経科学学会に転機が訪れたのが、2024年です。そう、僕が理事長を務めている日本生物学的精神医学会との、初めての合同大会が開かれたのです。それまで2割程度にとどまっていた疾患研究が、この年は、一気に3割越えとなりました。
疾患研究の増加に伴って、日本神経科学学会の理事の中にも、疾患研究者が増えてきました。当初は2%程度でしたが、今は15%くらいになっています。当初は神経内科領域の理事のみでしたが、2005年からは精神科領域の理事も加わりました。そして、2022年には、この学会として初めて、疾患研究者である山中宏二先生が、理事長に就任されたのです。
神経科学における精神疾患研究の課題
神経変性疾患の代表であるアルツハイマー病では、120年前に、老人斑、神経原線維変化、という病理学的所見が発見され、その生化学的解析からこれらの成分がアミロイドβ、リン酸化タウであることわかり、これらの遺伝子解析からモデル動物が作られ、アミロイドやタウを検出する検査法の開発、抗アミロイド薬の開発、と順調に研究が進んできました。
一方、精神疾患は、死後脳に顕微鏡で見える所見がないことからスタートしたため、こうした研究戦略では、研究を進めることができませんでした。
精神科臨床の中で可能な研究は、血液由来DNAを用いたゲノム研究と、脳画像研究が主体です。しかし、病気が宿るのは、細胞、シナプス、神経回路といった顕微鏡で観察する必要のある構造です。こうした研究は、主にモデル動物、iPS細胞由来神経細胞・脳オルガノイド、死後脳などでしか行えません。基礎研究と臨床研究の双方向的な連携が、精神疾患研究の推進のためには必須なのです。
過去20年、ゲノム研究ではSNP(一塩基多型)を調べるゲノムワイド関連研究、まれな変異を同定する全エクソーム/全ゲノム解析、デノボ変異、体細胞変異と、ゲノム要因の研究が進みました。
また、MRI研究では、J-ADNI、COCORO、Brain/Minds 2.0など、データーベース化が進み、多くの知見が得られました。
ゲノム研究で見出された遺伝子に改変を加えたマウスで、自閉スペクトラム症ではシナプスが出来やすく消えやすい、統合失調症では一部に大きなシナプス(スパイン)がある、うつ病ではシナプスが失われ、抗うつ治療で回復するなど、疾患毎に異なるシナプス病態がわかってきました。
新たな診断法の開発も進み、安静時結合MRI研究で見出された所見を診断に応用するための会社が設立され、臨床試験が進められています。
新たな治療法については、日本で開発されたアルツハイマー病の抗アミロイド薬をはじめとして、マウスの行動スクリーニングから見出されたドーパミンD2受容体阻害を介さない新規抗精神病薬など、次々と研究開発が進んでいます。
ゲノム研究で得られた原因遺伝子のリストを、整備されてきたデータベースと比較対照することで、その疾患の原因脳部位、原因細胞、発達中の病態が発生する時期などに加えて、同様の病態を引き起こす化合物、さらには病態を改善させる可能性のある化合物などを、インシリコ(コンピューター上)で、推定できるようにもなりました。
私たちの研究では、ゲノム研究で見出された、ミトコンドリアDNAの変異が生じるモデルマウスを作り、その脳病態を検討し、亡くなった患者さんの脳組織で確認することで、視床室傍核と双極性障害の役割を明らかにしつつあります。
神経科学によって、神経学と精神医学が統合していく未来は、決して不可能ではないでしょう。
基礎ー臨床連携シンポジウム
基礎ー臨床連携シンポジウムという、僕もメンバーである、「学術多様性委員会」が企画するシンポジウムでは、興味深い発表がなされました。